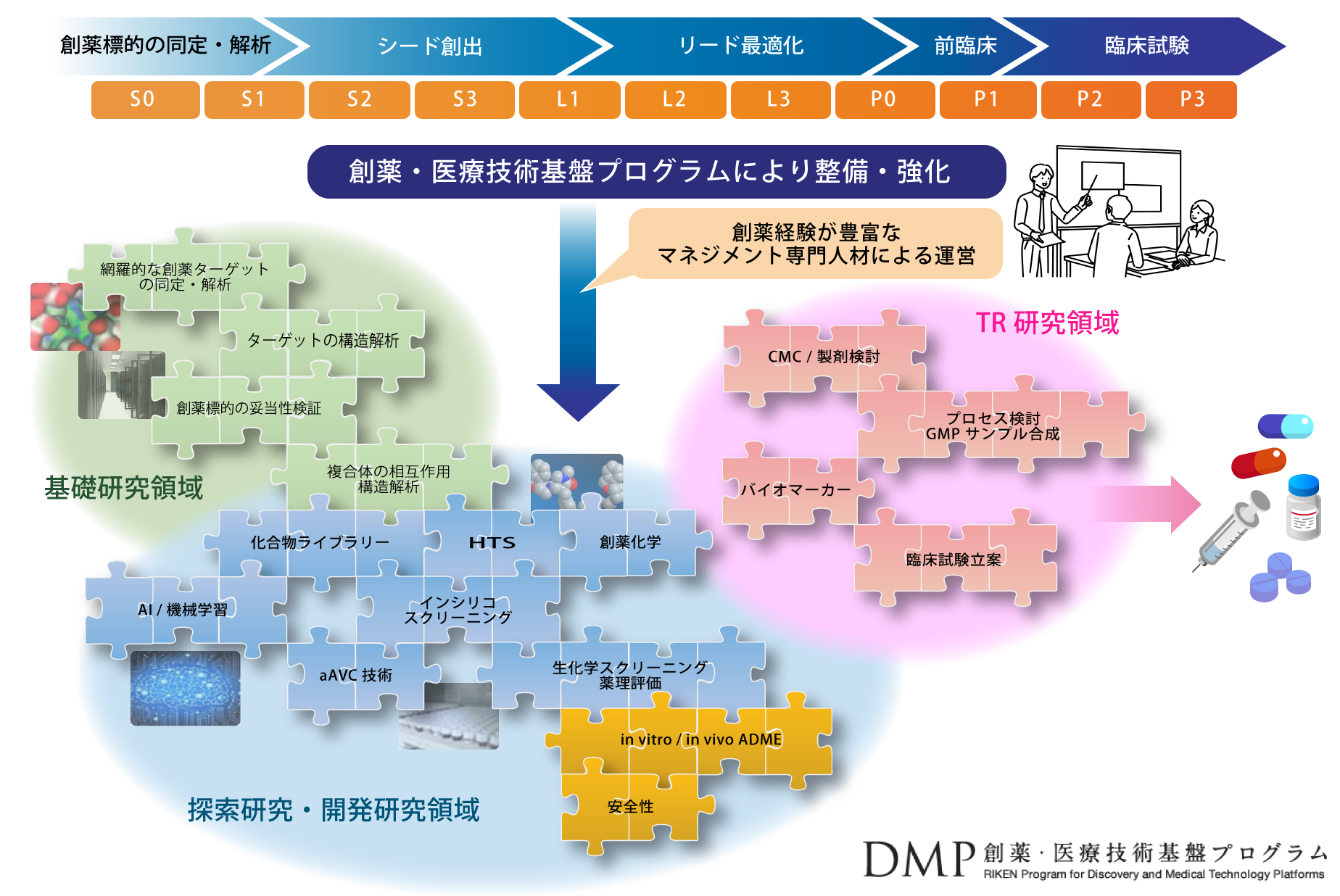
創薬分子設計
基盤ユニット
最新モデリング理論と統計理論を駆使した
高精度インシリコスクリーニング
創薬分子設計基盤ユニットでは、標的タンパク質の立体構造と既知阻害剤情報を用いて、最新のシミュレーションと人工知能技術の両面から精度の高いインシリコスクリーニングを実現しています。実験データを機械学習させ、量子化学計算等と組み合わせて予測すること、ADMETなどを考慮した最適化設計を可能していることが特長です。