戦略提携室
株式会社理研イノベーションとの連携のもと、当プログラムが推進する創薬テーマ・プロジェクトについて、企業や大学、外部研究機関との共同研究やライセンシング等のアライアンス部分を担当しています。
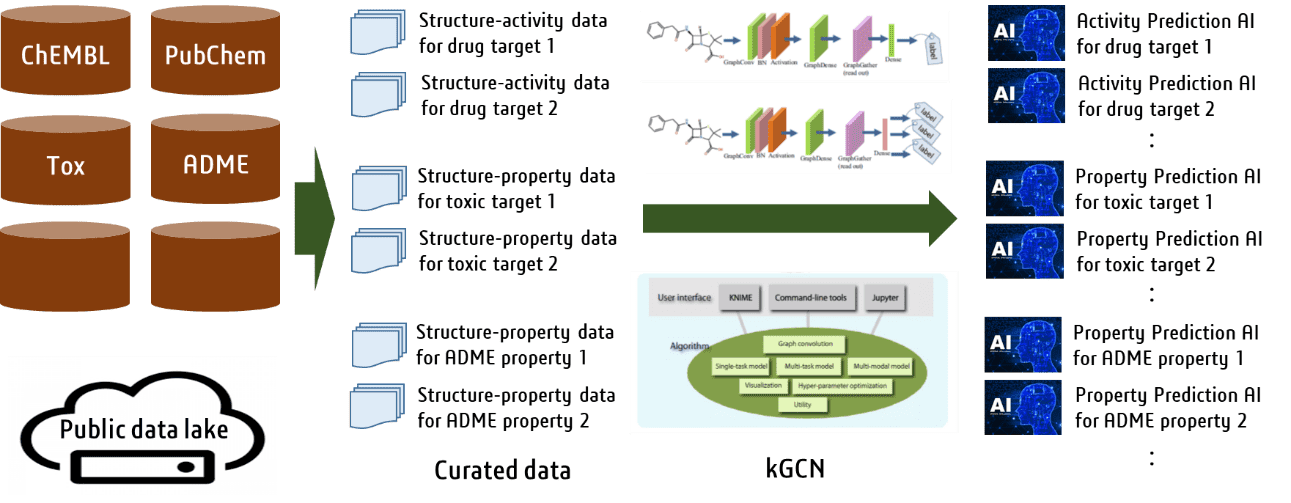
ChEMBL,PubChemなどに代表される数多くの創薬データベースが整備・公開され、様々な創薬標的に対する活性、毒性、薬物動態に関するデータが利用可能になってきました。我々は京都大学で開発されたグラフ畳込みニューラルネットワークシステムkGCN(J Cheminform.,2020,12,32)を中核に、これら膨大なデータを解析し、様々なAI予測システムを構築しています。
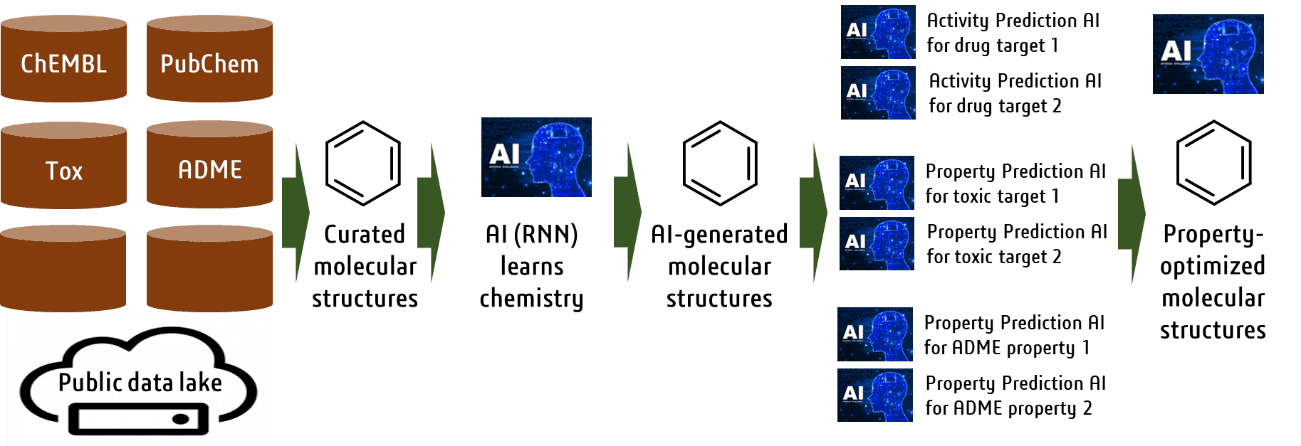
これまでの低分子医薬品は、人間がその化学構造を考え、創製してきました。創薬プロセスにおいてAIに新たな役割を担わせるため、我々は、化学構造を考えるプロセスをAI化し、医薬品として望ましい性質を持つ化学構造を、AIが人間に提示する研究を行っています。このため、ChEMBLなどに蓄積された膨大な数の化学構造をAIに学習させ、AIに”Chemistry”を教えました。さらに、様々なAI予測システムを応用し、医薬品として、より望ましい性質を有する可能性の高い構造を、AIにより効率的に生成させる研究を行っています。
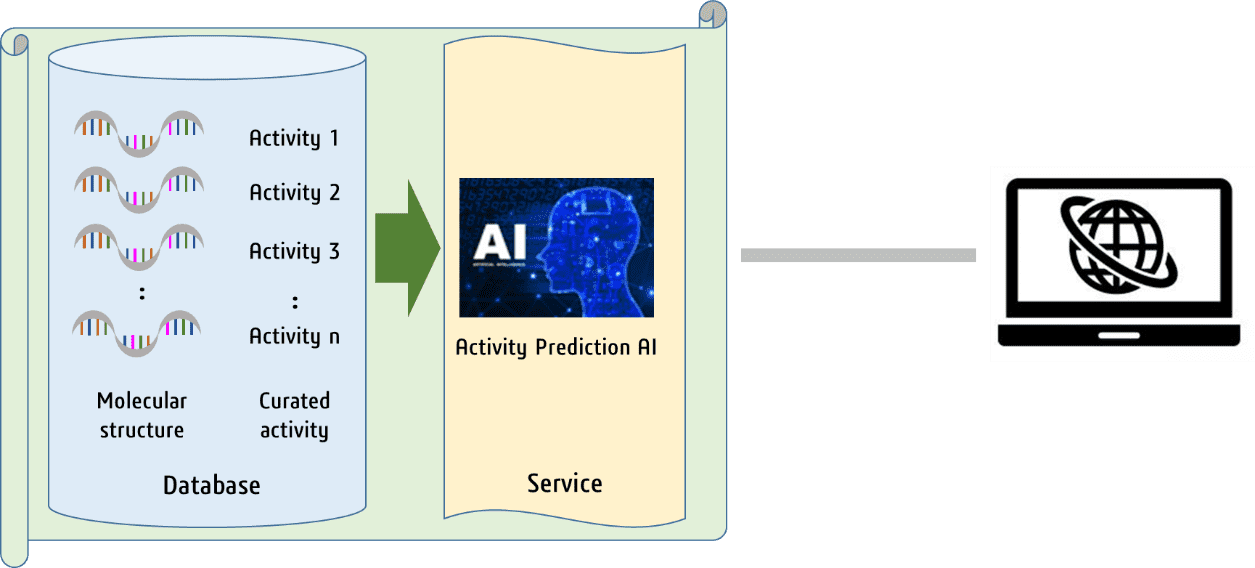
核酸医薬品は新しいモダリティーとして注目されており、いくつかの核酸医薬品が医薬品として認可され、使用され始めています。我々は、核酸医薬品の活性データを収集し、データベース化し、そのデータに対してAI技術を利用した予測モデルを作成し、これらを自由に使っていただけるよう、公開しようとしています。
薬剤は標的タンパク質に結合し、その活性を示します。薬剤がタンパク質に結合する際に、タンパク質周囲にある水(水和水)を追い出して結合する必要があります。ですので、水和水が薬剤に追い出されやすいのか、追い出されにくいのかは、薬剤が結合し、その活性を発揮するためにとても重要な情報です。
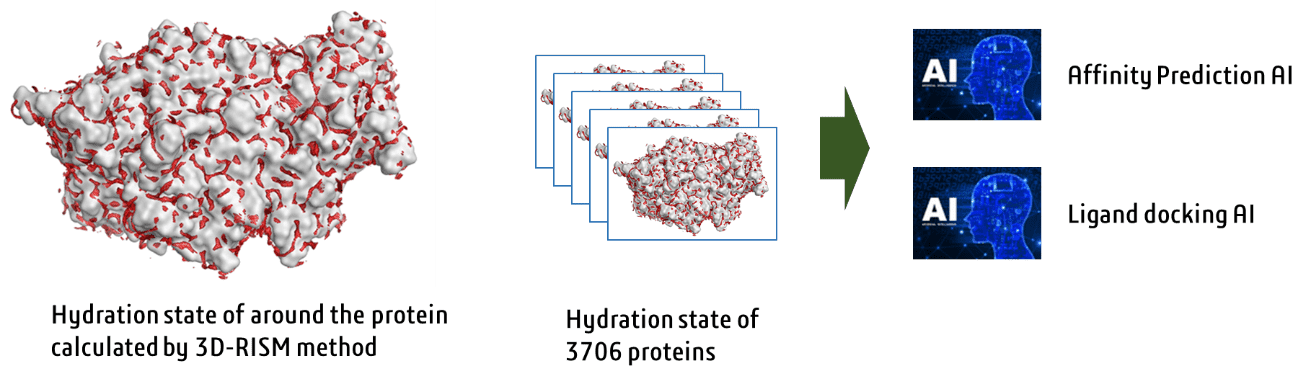
水和水の状態をシミュレーションできる技術が3D-RISM法です。我々は理研のスーパーコンピュータを用いて、3706種類のタンパク質について、3D-RISM法により水和水の状況を網羅的にシミュレーションしました (J. Comput. Chem., 2020, 41, 2406) 。これから、これらの情報とAIを利用して、薬剤の結合活性予測、ドッキング法の開発などを行っていきます。また、水和水の状況をAIにより瞬時に予測する方法論を開発しています。
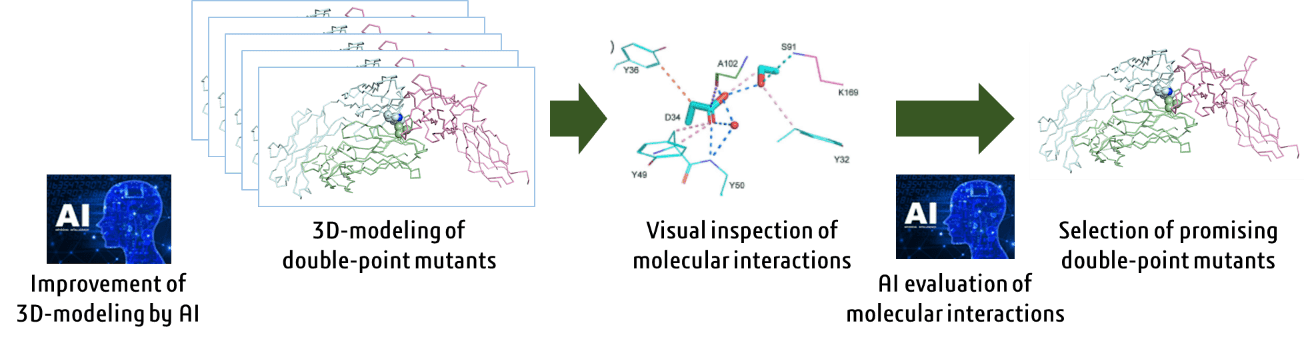
抗体医薬品は、革新的な医薬品の源泉の一つとなっています。抗体医薬品創製にあたっては、活性を有するリード抗体が取得された後、アミノ酸変異を行い、その活性、物性などを向上させていきます。通常はある一つのアミノ酸を変異させ、その活性、物性などの変化を見て、良かったものを組み合わせていきます。我々は、シミュレーション技術を使って、二つのアミノ酸を同時に変異させるという新しい方法を開発しました(Scientific Reports, 2020, 10, 17590)。
この方法では、膨大な数の二アミノ酸同時変異体の立体構造モデルを生成し、その立体構造に基づいて活性、安定性などが改善されるかどうかを評価する必要があります。現在、膨大な数の二アミノ酸同時変異体の立体構造モデルの作成は自動化されていますが、改善が必要であると考えており、AIを使用して手法を改良しています。また、二アミノ酸同時変異モデルに基づき、活性、物性が向上するかどうかの判断を人間が目視で実施しているので、これをAI技術で実現する研究に取り組んでいます。