多方向かつ段階的に進行する細胞分化における運命決定メカニズムの解明究領域略称:細胞運命制御
研究課題名
ヒストン脱メチル化酵素(KDM)による造血分化制御機構の解明
研究内容
本研究は、ヒストン脱メチル化酵素(KDMs)の造血制御機構および造血器腫瘍発症への関わりについて解明する。
最近の網羅的遺伝子解析から、急性骨髄性白血病(AML)や骨髄異形成症候群(MDS)といった造血器悪性腫瘍の発症に、基盤となる共通の分子メカニズムが存在することが明らかになってきた。その一つが、エピジェネティクス制御の破綻である。これまで、特にDNAメチル化やヒストンアセチル化が先行して注目を集め、Azacitidine(商品名ビダーザ、DNAメチル化阻害剤)やVorinostat(商品名ゾリンザ、ヒストン脱アセチル化酵素(HDAC)阻害剤)といった新規薬剤が、限定的ではあるが一定の成果を挙げてきた。この事実は、エピジェネティクス制御の破綻が造血器腫瘍の発症・維持に重要な役割を果たし、治療ターゲットに成り得ることを示している。
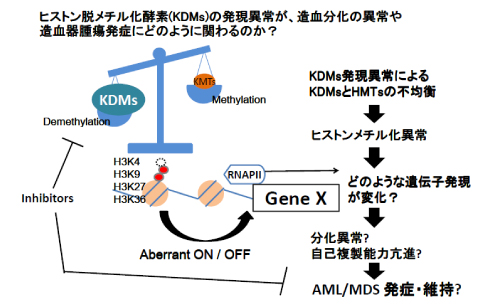
ヒストンメチル化修飾は、エピジェネティクス機構の一つで、特にヒストン3蛋白(H3)のリジン(K)残基のメチル化修飾が、遺伝子の発現調節に極めて重要で、ヒストンメチル化酵素(KMTs)と脱メチル化酵素(KDMs)によって精緻に可逆的に制御されるシステムである。AML/MDSでは、EZH2やMLLといったヒストンメチル化酵素に変異や転座が高頻度に集中していることが判明しており、こういった異常の機能解析が精力的に行われる一方で、HMTsの逆向き酵素であるKDMsの造血器腫瘍における役割はほとんど検討されていない。
最近我々は、新規に合成したKDM1A 阻害剤が、急性骨髄性白血病細胞の分化を促進して、増殖抑制することを見出した(未発表データ)。これは、ヒストン脱メチル化酵素の異常が、造血分化の異常を引き起こし、逆にその是正が、有望な白血病治療の治療法になりうることを示唆している。
そこで、我々は、造血器腫瘍で重要な役割を果たしていると考えられるいくつかのKDMsに関して、その発現増強もしくは低下が、造血細胞分化や、白血病の発症・維持にどのように寄与するのか、そのメカニズムを解析し、将来の白血病新規治療薬につながるような基盤的な研究を目指す。
主な論文
- 河原 真大
-
Kawahara M, Pandolfi A, Bartholdy B, Barreyro L, Will B, Roth M, Okoye UC, Todorova T, Figueroa ME, Melnick A, Mitsiades CS, and *Steidl U.
H2.0-like homeobox (HLX) regulates early hematopoiesis and promotes acute myeloid leukemia.
Cancer Cell. 22: 194-208, 2012Steidl C, Shah SP, Woolcock BW, Rui L, Kawahara M, Farinha P, Johnson NA, Zhao Y, Telenjus A, Ben Neriah S, McPerson A, Meissner B, Okoye UC, Diepstra A, van den Berg A, Sun M, Leung G, Jones SJ, Connors JM, Huntsman DG, Savage KJ, Rimsza LM, Horsman DE, Staudt LM, Steidl U, Marra MA, and *Gascoyne RD.
MHC ClassII Transactivator CIITA is a recurrent gene fusion partner in lymphoid cancers.
Nature. 471: 377-381, 2011Kawahara M, *Hori T, Chonabayashi K, Oka T, Sudol M, and Uchiyama T.
Kpm/Lats2 is linked to chemo-sensitivity of leukemia cells through the stabilization of p73.
Blood. 112: 3856-3866, 2008 - 鈴木 孝禎
-
*Suzuki T, and Miyata N.
Lysine demethylase inhibitors.
J. Med. Chem. 54: 8236-8250, 2011*Suzuki T.
Explorative study on isoform-selective histone deacetylase inhibitors.
Chem. Pharm. Bull. 57: 897-906, 2009