多方向かつ段階的に進行する細胞分化における運命決定メカニズムの解明究領域略称:細胞運命制御
研究課題名
mTOR複合体1を介した細胞分化制御機構の解明
研究内容
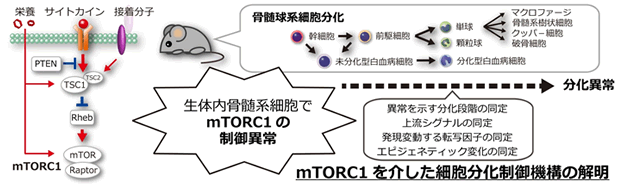
Mammalian target of rapamycin (mTOR)は、抗生物質・免疫抑制剤ラパマイシンの標的として同定されたKinaseであり、mTOR複合体1(mTORC1)を形成し、様々な細胞外シグナルにより活性化する。近年の精力的な研究により、多くの生命現象に関わることが知られるようになり、生命科学分野の中で最も注目されているシグナル伝達分子の1つである。
mTORC1に関する研究の多くがラパマイシンとその誘導体による効果に依存したものであるが、mTORC2の発見後には、細胞種によってはmTORC2を阻害することが示されるなど、ラパマイシンに依存したmTORC1の研究には限界が生じている。またmTORC1の下流分子はグローバルな翻訳機構を制御するとされ、均一な性質を持つ細胞株を用いたin vitroでの実験が先行して行われてきたため、in vivoで多方向かつ多段階的に起こる各分化段階での役割の違いについては明らかではない。
申請者はこの数年間、mTORC1活性化に関わる分子群の遺伝子改変マウスを樹立・解析し、主に造血幹細胞制御における役割の解明に取り組んできた。その研究の成果として、「mTORC1の活性変動は細胞の分化に大きく影響を及ぼす」という知見を得た。
本研究では、in vivoの細胞分化制御におけるmTORC1活性の役割を明らかにする目的で、細胞系譜と分化メカニズムの研究の最も進んでいる骨髄球系細胞の分化に焦点を当てて解析を進める。
主な論文
- 星居 孝之
-
Naka K†, Hoshii T†, Muraguchi T, Tadokoro Y, Ooshio T, Kondo Y, Nakao S, Motoyama N, *Hirao A. (†equally contribution)
TGFβ-FOXO signalling maintains leukaemia-initiating cells in chronic myeloid leukaemia
Nature. 463: 676-680, 2010.Tamase A, Muraguchi T, Naka K, Tanaka S, Kinoshita M, Hoshii T, Ohmura M, Shugo H, Ooshio T, Nakada M, Sawamoto K, Onodera M, Matsumoto K, Oshima M, Asano M, Saya H, Okano H, Suda T, Hamada J, Hirao A.
Identification of tumor-initiating cells in a highly aggressive brain tumor using promoter activity of nucleostemin
Proc Natl Acad Sci U S A. 106: 17163-17168, 2009.Hoshii T, Takeo T, Nakagata N, Takeya M, Araki K, *Yamamura K.
LGR4 regulates the postnatal development and integrity of male reproductive tracts in mice
Biol Reprod. 76: 303-313, 2007.