低分子創薬
2010年の本プログラムスタート以来、低分子創薬基盤を充実させることに力を入れてきました。低分子化合物ライブラリーのスクリーニング、ヒット化合物からの合成を行い、理研の強みであるタンパク質解析、先端計算化学、創薬分子設計を担当する創薬基盤(研究センターに設置)が協働して、新規創薬標的に対する低分子化合物創薬を推進しています。
創薬とは、疾患の原因となる分子を同定し、それを適切に制御するモダリティ(低分子、抗体、核酸など)を開発し医療へとつなげる取り組みです。創薬・医療技術基盤プログラム(DMP)では、優れた基礎研究の成果から革新的な医薬品の創出を目指すとともに、創薬研究を支える基盤の整備とその実装に取り組んでいます。
さらに、放射性医薬品やAI、量子コンピュータを活用したデータ駆動型創薬など、理研の最先端科学技術を基盤とする独創的な創薬研究を推進しています。企業や医療機関との連携のもと、基礎研究の成果を医療へと橋渡しし、次世代医療への貢献を目指します。

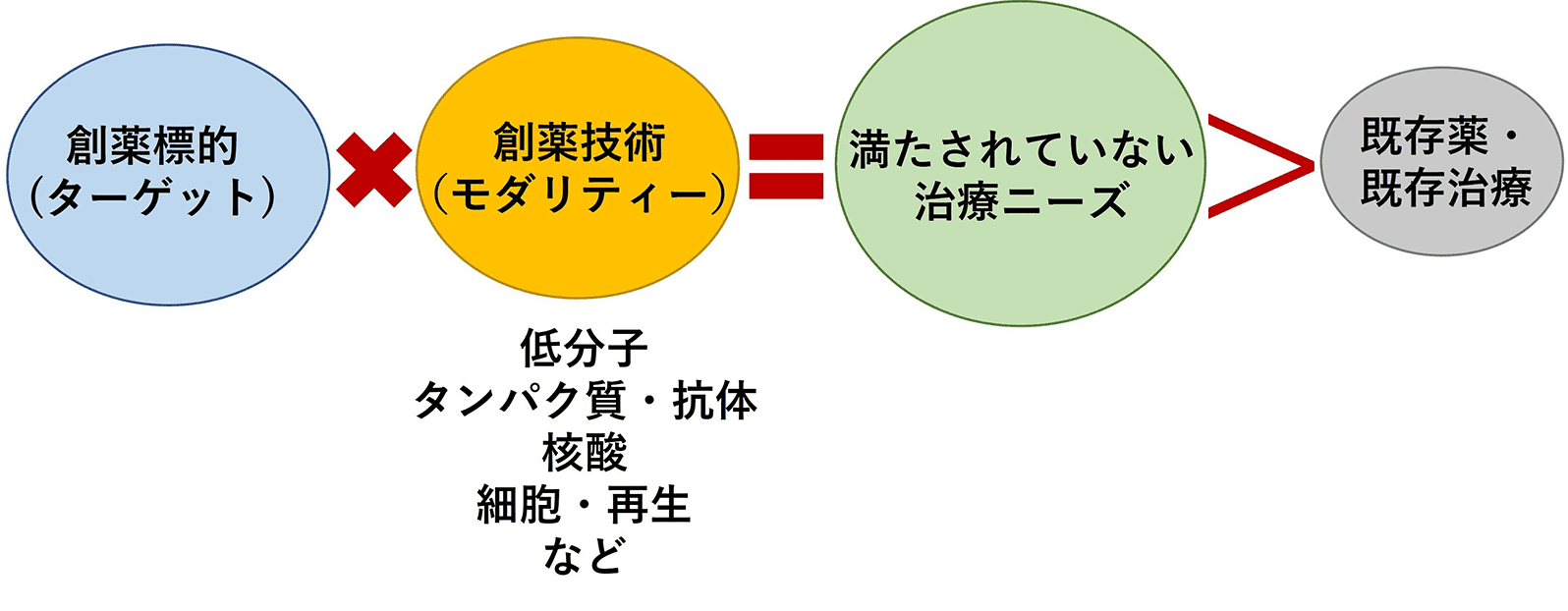
創薬・医療技術基盤プログラムが目指す創薬では「新たな創薬標的」と「新しい創薬技術」の掛け合わせにより、「満たされていない治療ニーズ」を満たすために、既存の治療薬や治療方法を超える製品を創出します。
理研および大学等のアカデミアの研究機関の新規創薬標的を創出するバイオサイエンスに期待し、病気の原因を解明し、治療薬創製の標的としての可能性を評価、分析します。新薬としての実用化に必要な研究の方向性、開発計画および薬事承認に必須なプロセスを支援します。
創薬標的としては治療満足度が低い疾患の新しい治療方法、創薬標的が未知でこれまでアプローチが難しかった疾患(希少疾患、感染症、免疫疾患、中枢疾患、等)に焦点をあてて支援します。
2010年の本プログラムスタート以来、低分子創薬基盤を充実させることに力を入れてきました。低分子化合物ライブラリーのスクリーニング、ヒット化合物からの合成を行い、理研の強みであるタンパク質解析、先端計算化学、創薬分子設計を担当する創薬基盤(研究センターに設置)が協働して、新規創薬標的に対する低分子化合物創薬を推進しています。
人工アジュバントベクター細胞 (aAVC) 技術のような、創薬にパラダイムシフトを促す新規技術の創出を支援します。aAVCは、現在注目されているCAR-T療法の次世代を担う技術として位置付けています。そのような新たな細胞・再生医療技術の研究開発を目指します。
理研独自のタンパク質工学および抗体作成技術を基盤とする創薬を支援します。また、既に治療薬は存在していますが、最適な創薬技術に至っていない医薬品の研究開発を、理研の研究センターとの協働により推進します。
創薬に応用可能な革新的な技術を積極的に探索し、創薬標的との相乗効果を検討します。
医薬品の研究開発および実用化において近年の外部の環境は変化しています。オープンイノベーションの重要性が認識され、その環境整備が進む中、新規創薬標的ならびに新規創薬技術に対する期待から、理研を含めて大学等の研究機関(アカデミア)の研究成果を活用した創薬に注目が集まっています。
医療技術は多岐に渡りますが、創薬研究のプロセスは、低分子医薬の場合、疾患ターゲットやメカニズムの特定、疾患に関係するタンパク質等に作用するリード化合物の探索・同定、リード化合物の最適化、薬効の確認試験、安全性の確認などの非臨床試験を経て、臨床試験に進みます。細胞・再生医療であれば、特定の細胞や組織の創出、これらの機能確認、安全性の確認の試験などの流れになります。
創薬・医療技術基盤プログラムは、理研の研究センターから生み出される最新のサイエンスを生かし、創薬・医療技術基盤プラットフォームにつなげる役割を担っています。マトリックスマネジメントにより、ポートフォリオマネージャーがテーマ・プロジェクトを推進し、企業・ベンチャーに実用化を託します。