研究内容
- 再生医療工学
- ナノメディシン
- 分子診断、分子イメージング
- 核酸・ペプチド工学
- ナノマテリアル、ナノ界面
1.1.成長因子固定化材料、結合性成長因子
再生医療工学、組織工学では、幹細胞、細胞外マトリックス、成長因子の三位一体の制御が必要となります。我々は1990年に成長因子を化学的に材料上に固定化しても細胞機能を制御できるばかりか、溶解状態の成長因子より長時間にわたり細胞活性化を維持できることを見出しました。最近では、化学的固定化だけでなく、タンパク質工学やバイオ直交化学、進化分子工学を応用した結合性タンパク質を調製しています。また、三次元マトリックスに結合させるか、あるいは直接投与して、生体組織の再生に役だつことを明らかにしています。そして有機材料だけでなく、金属やセラミックスなど無機材料への固定化を含め、研究を展開しています。
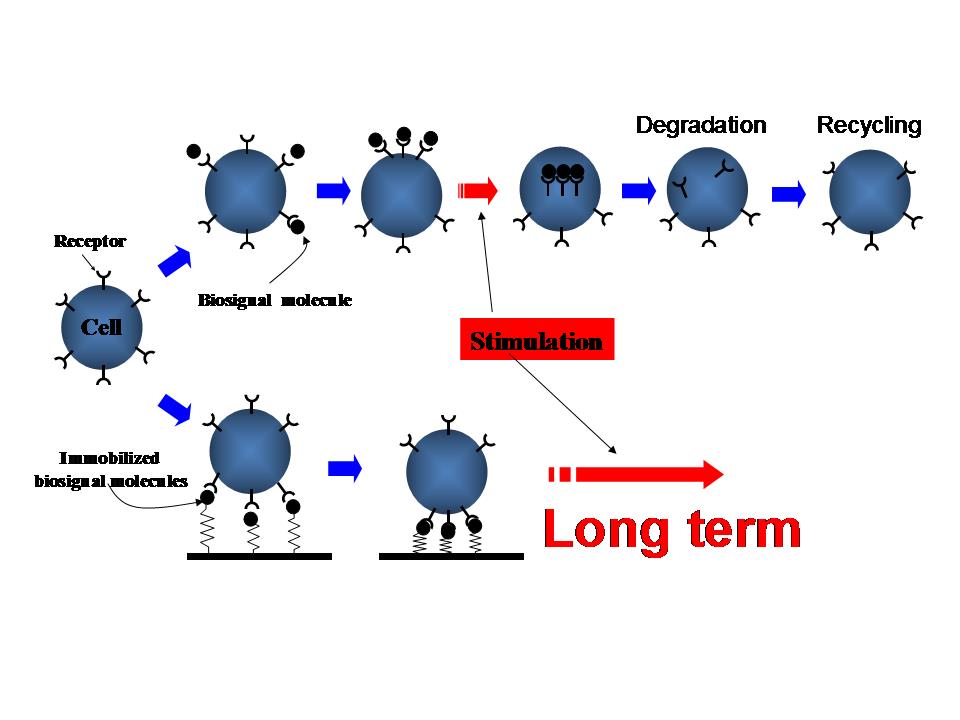 Figure 1 Long-term activation by immobilized biosignal molecule
Figure 1 Long-term activation by immobilized biosignal molecule
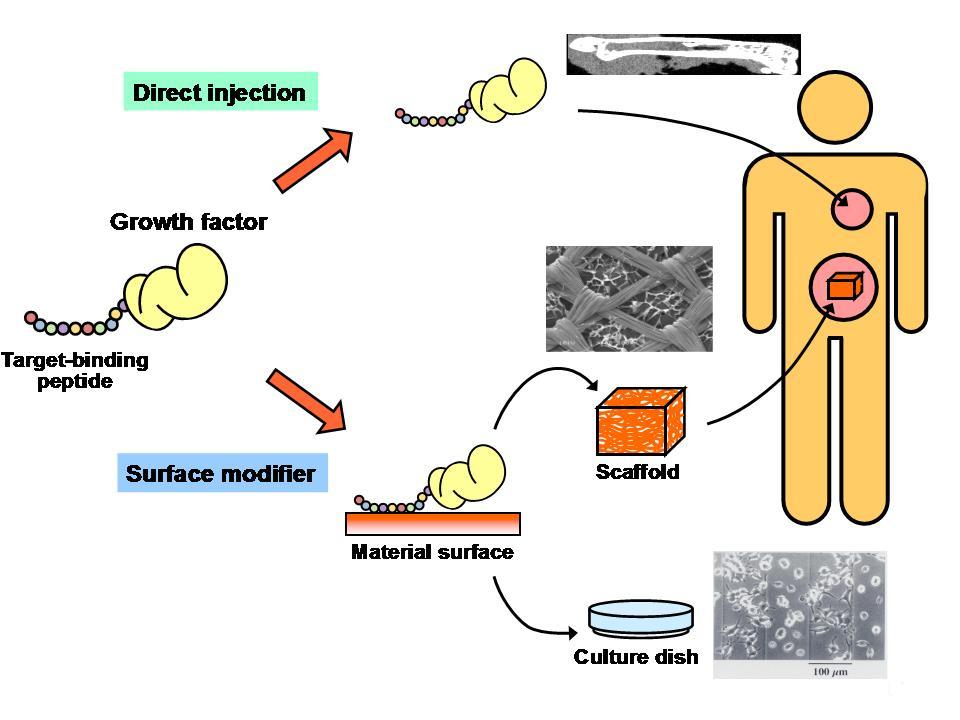 Figure 2 Applications of engineered growth factors
Figure 2 Applications of engineered growth factors
1.2.光反応性高分子
化学的に固定化した成長因子の活性を調べるために、成長因子をマイクロパターン状に固定化するようになりました。この方法を用いることで、固定化成長因子が作用しているかどうかを、固定化されていない領域と比較することで、一目瞭然となりました。様々なUV反応性高分子を調製すると同時に、可視光硬化型高分子への応用を検討しています。
 Figure 3 Micropatterned mask (upper), micropattern immobilizations of protein and staining with CBB (middle), and cell culture on micropatterned surfaces (lower)
Figure 3 Micropatterned mask (upper), micropattern immobilizations of protein and staining with CBB (middle), and cell culture on micropatterned surfaces (lower)
1.3.幹細胞(ES細胞、iPS細胞)培養
固定化成長因子は、様々な局面で応用可能です。多くの幹細胞はフィーダー細胞とともに培養することが必要になります。しかし、フィーダー細胞を使う手間や、夾雑物を考えると、必要となる成長因子だけを固定化した基材が開発されれば、再生医療の発展に大きく寄与します。本研究室では、幹細胞培養のために成長因子を固定化する研究、さらに、フィーダー細胞を化学的に固定化して利用する研究を進めています。
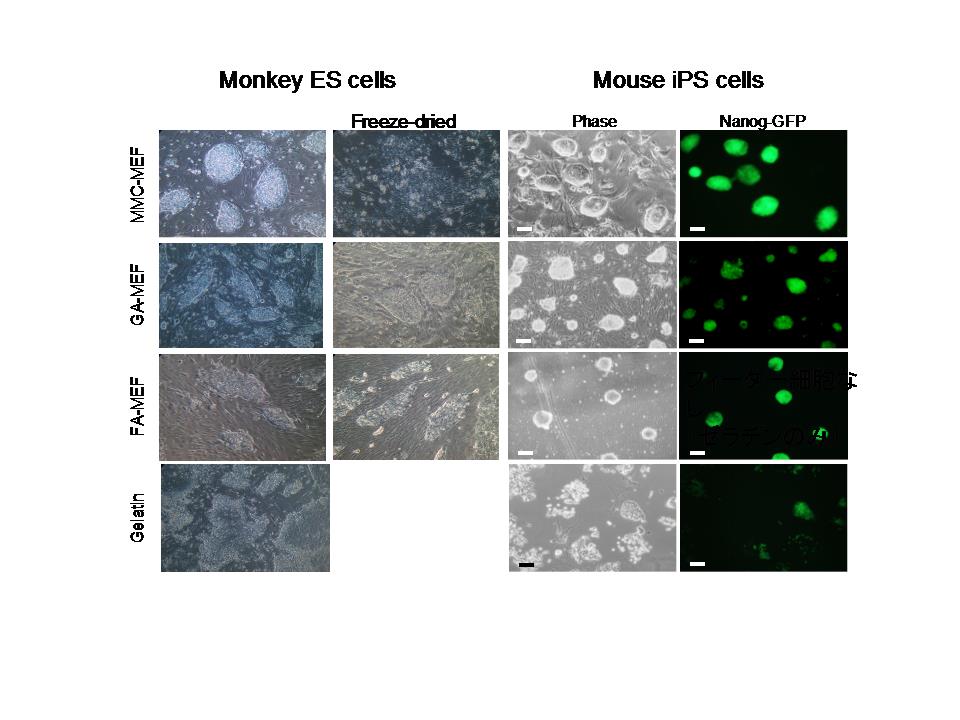 Figure 4 Culture of monkey ES and mouse iPS cells on mitomycine C-treated mouse embryonic feeder (MMC-MEF), glutaraldehyde-fixed MEF (GA-MEF), formaldehyde-fixed MEF (FA-MEF), and gelatin.
Figure 4 Culture of monkey ES and mouse iPS cells on mitomycine C-treated mouse embryonic feeder (MMC-MEF), glutaraldehyde-fixed MEF (GA-MEF), formaldehyde-fixed MEF (FA-MEF), and gelatin.
1.4.MEMSによる細胞加工(リプログラミング)
体性細胞を初期化して未分化状態にもどす方法には、核移植、細胞融合、そして遺伝子導入があります。iPS細胞は、遺伝子導入で成功した顕著な例です。細胞融合の場合には、4倍体ができる問題があります。そこで、これをMEMS技術で回避する方法の開発に前田バイオ工学研究室と取り組んでいます。
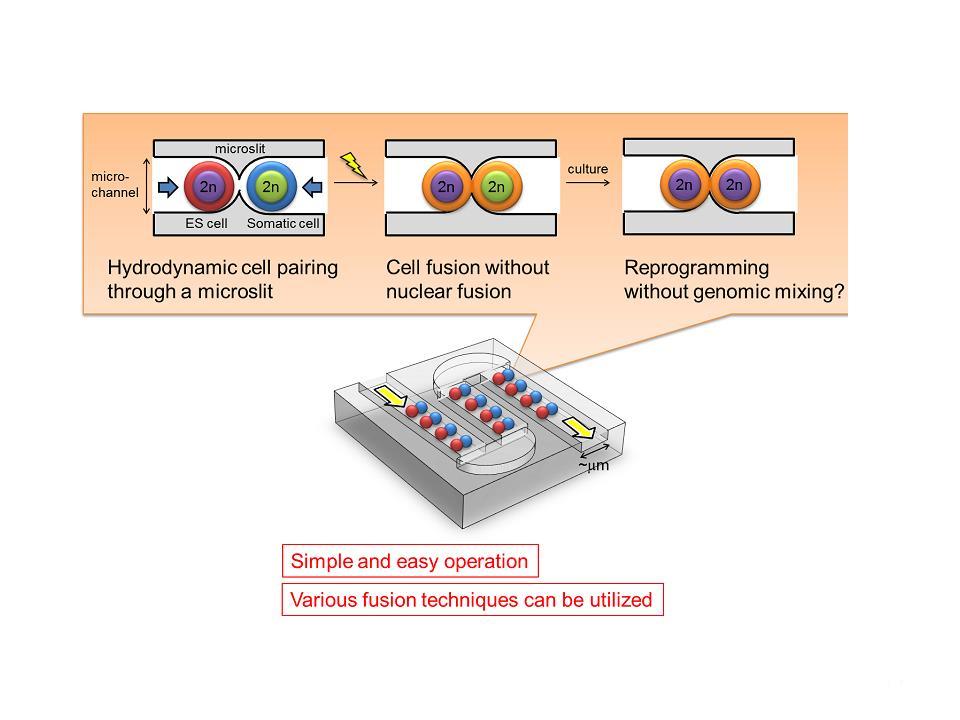 Figure 5 Cell manipulations by Micro Electro Mechanical Systems (MEMS)
Figure 5 Cell manipulations by Micro Electro Mechanical Systems (MEMS)
2.1.siRNAデザイン
siRNA(small interfering RNA)とは21-23塩基対から成る低分子二本鎖RNAで、RNA干渉(RNAi)と呼ばれる現象に関与しており、mRNAの破壊によって配列特異的に遺伝子の発現を抑制します。その配列特異的な遺伝子発現抑制効果から、これまでに治療が困難であった病気への治療法として期待されますが、RNAの生体内不安定性や細胞内への取り込みの難しさが、その妨げになっています。その問題を克服するために、私たちはRNAのナノ構造と生物活性の相関に注目し、独自のRNAナノテクノロジー研究を展開しています。
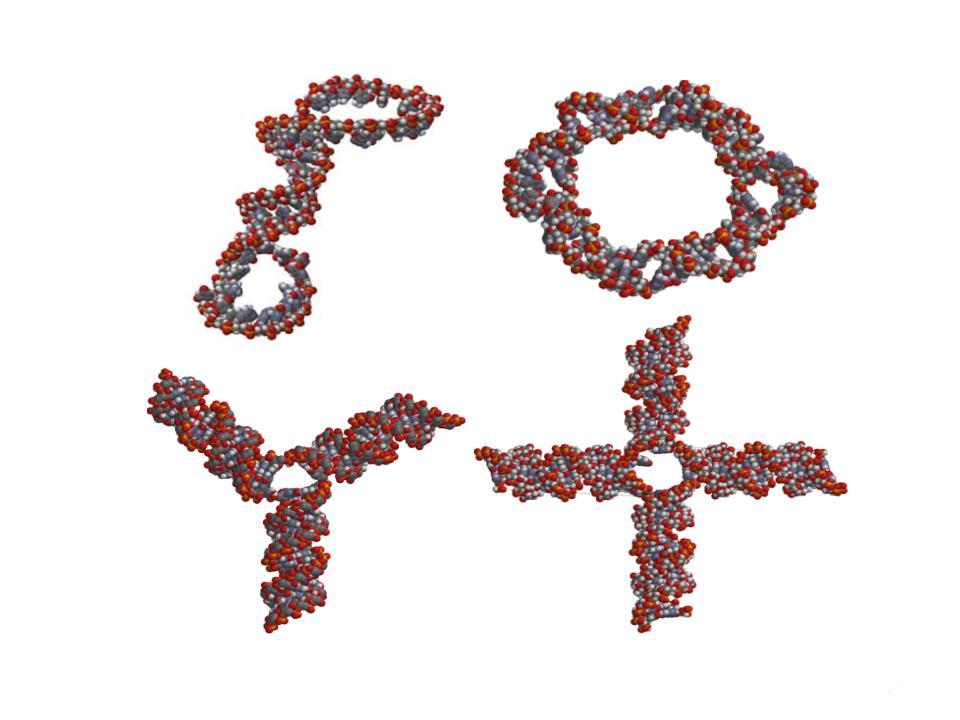 Figure 6 Nano-structured siRNAs
Figure 6 Nano-structured siRNAs
2.2.ドラッグ・デリバリー・システム
新しい医薬を作るのと同時に、医薬を効率よく患部に送達することが重要な研究課題となっています。医療チームを乗せた潜航艇を縮小して体内に注入し、脳の内部から治療する1966年公開のSF映画「ミクロの決死圏」を分子レベルで実現すべくsiRNA、ワクチン、医薬などの高効率な送達のための新しい基材の開発を行っています。
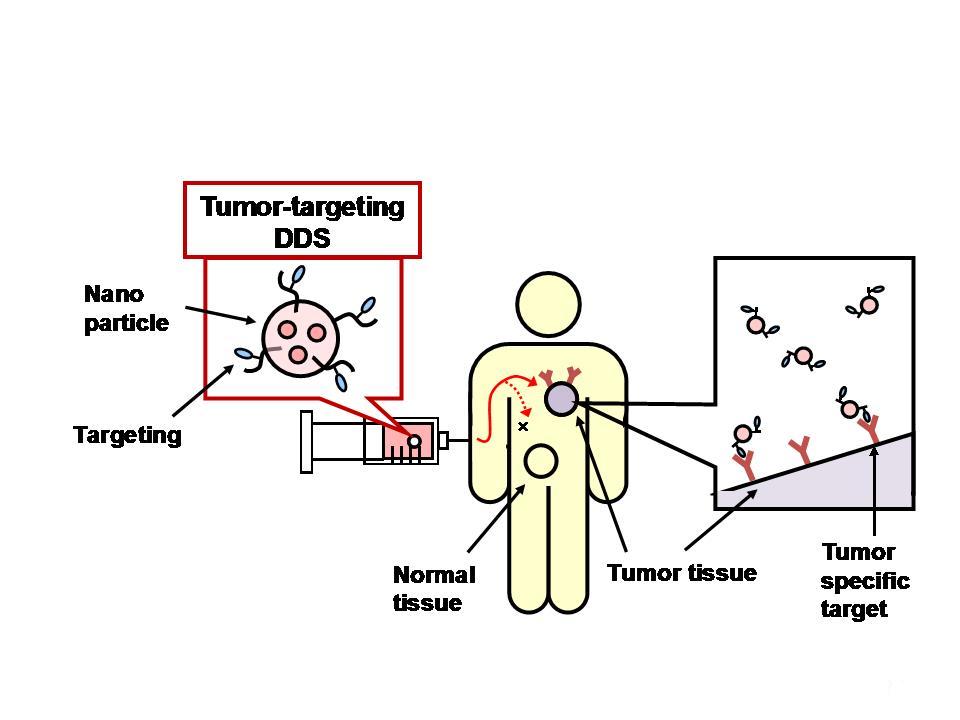 Figure 7 An example of drug delivery system
Figure 7 An example of drug delivery system
3.1.マイクロアレイ型タンパク質チップ
1990年代からマイクロアレイ型のバイオチップの開発が始まり、現在では、DNAチップマイクロアレイが科学研究だけではなく、医療でも使われるようになっています。しかし、まだタンパク質マイクロアレイについては、実用化されていません。そこで、光固定化法を用いた「なんでも固定化法」を開発しました。この方法を用いることで生体分子をはじめ様々な有機分子のマイクロアレイ固定化が可能となりました。アレルゲン、自己抗原、ウイルスを固定化することにより、各々アレルギー、自己免疫疾患、免疫履歴などの検出、診断に応用できることを明らかにしてきました。
 Figure 8 Detection image of microarray chip
Figure 8 Detection image of microarray chip
 Figure 9 Automated microarray systems
Figure 9 Automated microarray systems
3.2.遺伝子、タンパク質の検出分子プローブ
遺伝子やタンパク質の検出は様々な分野で重要です。遺伝子検出では、独自に化学反応(求核置換反応や還元反応)に基づいて 蛍光発光する人工核酸プローブを開発し、細胞内RNAの定量的イメージング解析に成功し、RETF (REduction Triggered Fluorescence)プローブと名付けました。細胞内で化学的なシグナル増幅反応を起こすことにより、高感度な検出が可能となります。 タンパク質検出では、癌マーカーとしても知られるグタチオンSトランスフェラーゼ(GST)の検出ができるプローブを開発しました。GSTの反応基質となることで脱保護される保護基を考案し、 スウェーデン・カロリンスカ研究所のグループと共同でGSTを細胞内で直接イメージングできる蛍光プローブを開発しました。さらに、独自の分子メカニズムに基づき、生物発光プローブ、MRIプローブや、抗癌剤のプロドラックも開発しました。 また、後述する進化分子工学で新しい蛍光発生検出プローブの創製に取り組んでいます。これらプローブを用いて、ケミカルバイオロジー研究、さらに診断、創薬へと大きな研究展開が可能となります。
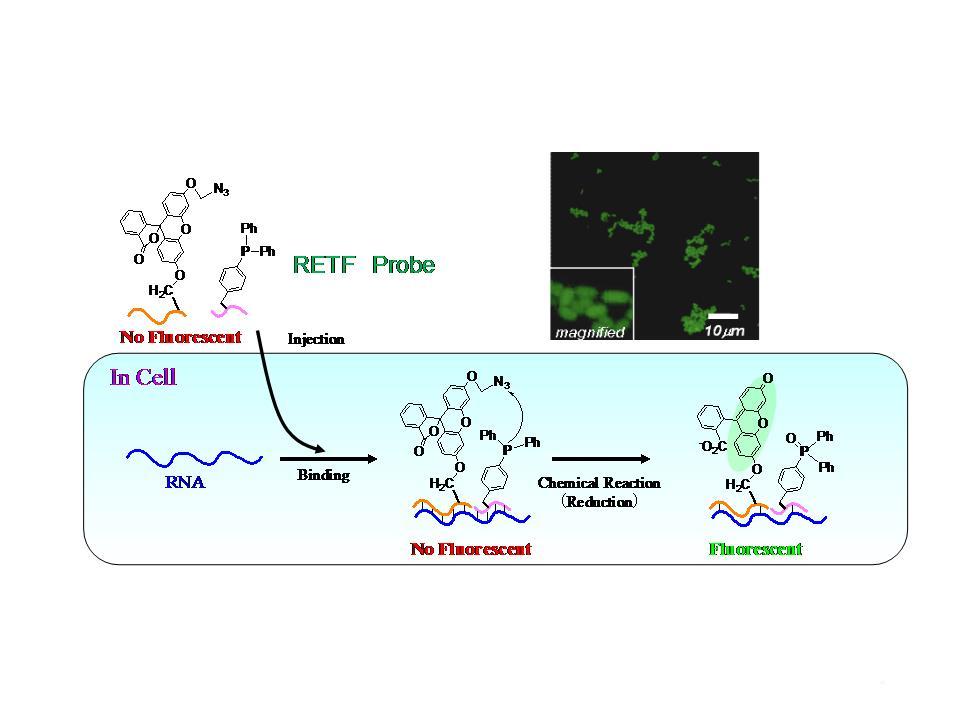 Figure 10 Mechanism of developed RETF probe
Figure 10 Mechanism of developed RETF probe
4.1.生体系を利用した精密高分子合成と機能性
生体では、核酸情報に基づいてリボソームがアミノ酸をつないでタンパク質を合成します。この過程を「翻訳」といいます。近年、試験管内でこの「翻訳」を比較的に容易に行えるようになってきました。そこで、tRNAに天然アミノ酸以外のものを担持させたり、mRNAを環状にしたりして、生体系を利用した新しい精密高分子合成を研究しています。 また、生体高分子と合成高分子をハイブリッド化することにより新しい機能性を付与することも可能です。両親媒性のポリエチレングリコールを結合した抗体やDNAは有機溶媒に溶解して機能を発揮することが明らかになりました。
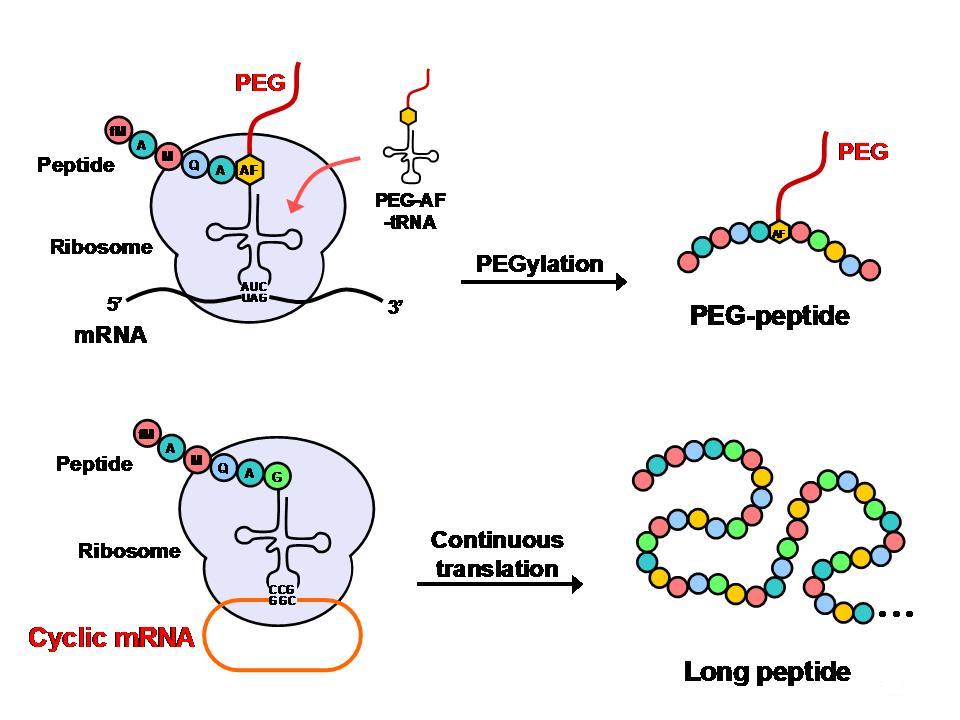 Figure 11 Ribosomal syntheses of bioorthogonal proteins
Figure 11 Ribosomal syntheses of bioorthogonal proteins
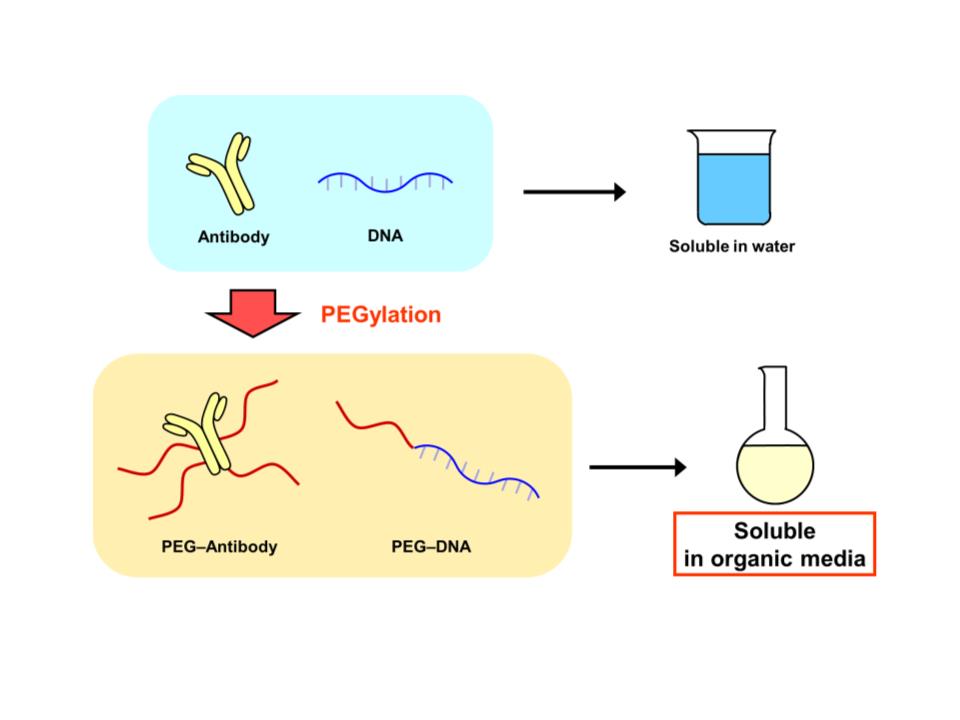 Figure 12 PEGylated antibody and oligonucleotides are active in organic media
Figure 12 PEGylated antibody and oligonucleotides are active in organic media
4.2.進化分子工学による機能性高分子の合成
1990年前後から進化分子工学という手法が開発されました。これは、ダーウィン進化の「突然変異」、「自然淘汰」、「増殖」の各プロセスを、各々「ランダム配列の生体分子ライブラリー」、「アフィニティ選別」、「PCR増幅」に置き換えた方法で標的に特異的に結合する生体分子(DNA、RNA、あるいはペプチド)を得ることができます。このように得られた結合性の生体分子をアプタマーと呼びます。 本研究室では、この手法を使い、カーボンナノマテリアルやその他の無機材料にも結合するアプタマーの探索を行うとともに、この方法論を化学的に拡張して、非天然核酸や非天然アミノ酸も導入可能にし、単に結合するだけでなく、新しい機能を付与することを行っています。 進化分子工学の拡張によって得られる新しいアプタマーの例として、光異性化するアゾベンゼンを導入した核酸アプタマーやペプチドアプタマーを作りだし、新しいホスト・ゲスト化学分野を開拓しています。
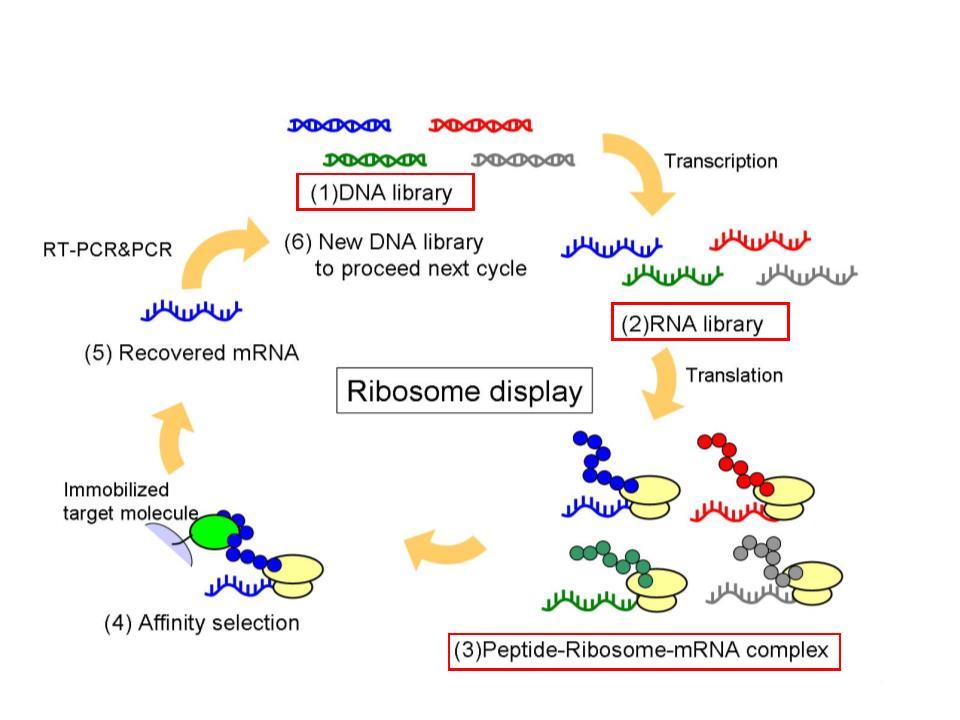 Figure 13 Ribosome display
Figure 13 Ribosome display
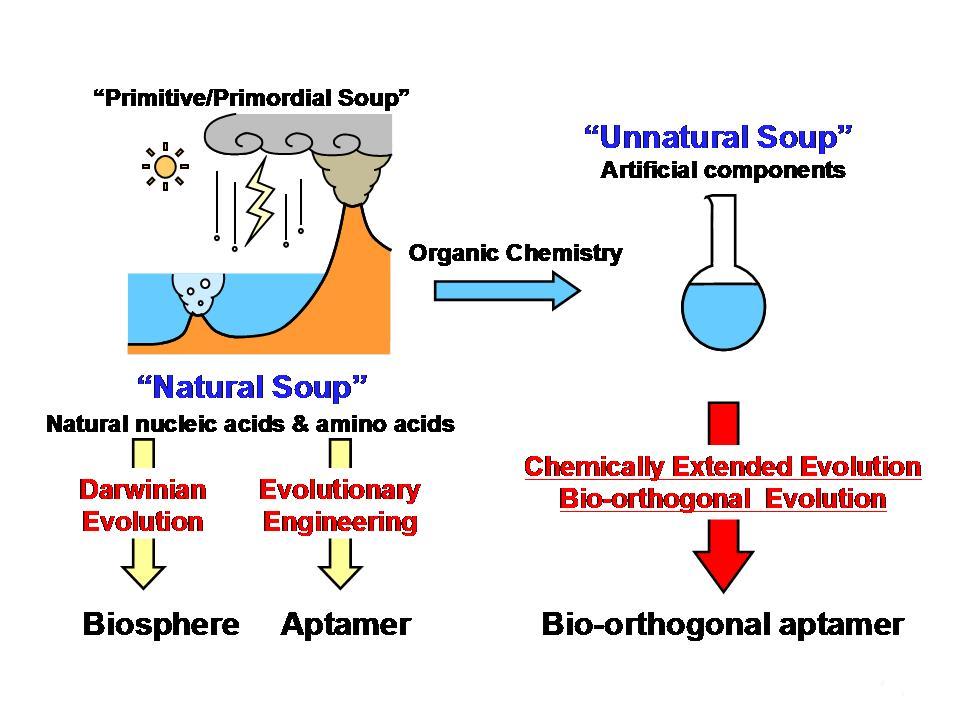 Figure 14 Extension of molecular evolutionary engineering
Figure 14 Extension of molecular evolutionary engineering
5.1.刺激応答性高分子
pH、熱、光などいろいろな刺激に応答してコンフォメーション変化する高分子が知られています。本研究室では、新しい刺激応答性高分子を合成し、その機能を分子レベルで探るとともに、その機能を利用した新しい応用を検討しています。
5.2.材料表面処理(濡れ性制御、生体不活性表面)
材料表面の親水性を制御して水滴の移動を表面加工により制御できるようにしました。また、タンパク質や細胞が接着しない新しいタイプの高分子材料をさまざま合成し、有機材料、無機材料を問わず、いろいろな材料の表面処理を行っています。
 Figure 15 AFM images of micropatterned polyethylene glycol on (a) titanium, (b) glass, and ThermanoxTM
Figure 15 AFM images of micropatterned polyethylene glycol on (a) titanium, (b) glass, and ThermanoxTM
5.3.ナノファイバー
エレクトロスピニング法で生分解性高分子からなるナノファイバーを作り、その応用展開を図っています。
 Figure 16 SEM micrographs of electrospun fibers of PHBV/gelatin (50/50) using TFE solutions as a function of concentration. (a) 2 wt%, (b) 4 wt%, (c) 6 wt%, (d) 8 wt%.
Figure 16 SEM micrographs of electrospun fibers of PHBV/gelatin (50/50) using TFE solutions as a function of concentration. (a) 2 wt%, (b) 4 wt%, (c) 6 wt%, (d) 8 wt%.
