生物情報基盤構築チーム, 先端技術基盤部門, 基幹研究所, 理化学研究所
細胞内ロジスティクスのデジタル解析
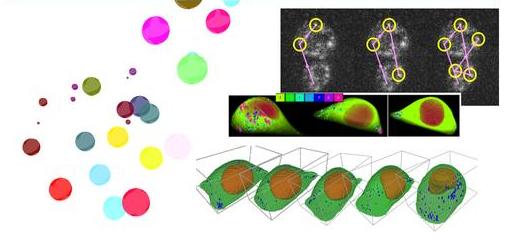
細胞内ロジスティクス観察画像データ
Contents
- メラノソーム輸送
- 緑色蛍光ラテックスビーズの結合・取り込み
- 刺激に応じて発光する細胞
- 細胞質細胞核分裂の4次元観察
- コレステロールプローブのエンドサイトーシス
- 様々な条件下でのオートファゴソーム輝点
- オートファゴソーム形成因子
- back to 細胞内ロジスティクスのデジタル解析
- back to 平成21年度 文部科学省 新学術領域研究:細胞内ロジスティクス 理論研究区分公募内容
-
平成21年度科研費公募「細胞内ロジスティクス」の参考資料としてのデータ追加は終了しましたが、今後も細胞内観察画像を本URLに追加予定です。
メラノソーム輸送
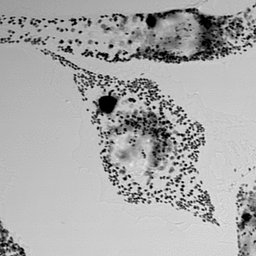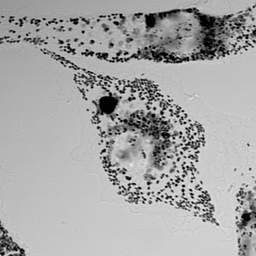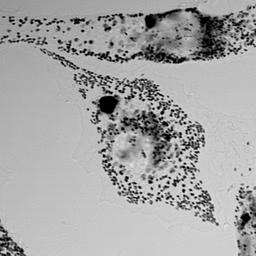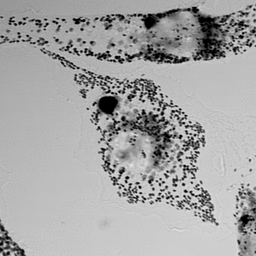
光学顕微鏡タイムラプス観察画像例
メラノソーム輸送
(東北大学 福田光則 先生提供)
以下のデータは東北大学 福田光則 先生提供の正常及びGriscelli症候群メラノサイトにおけるメラノソーム輸送の明視野顕微鏡観察画像です。その動態パターンの自動認識・解析が求められています。福田先生には定量解析の学術意義として下記説明文を頂きました。
メラノサイトにおけるメラノソームの動態:メラノソームはメラニン色素を含むため、明視野顕微鏡での観察が可能であり、一つ一つの動きを追跡する事が出来ます。これまでの研究では細胞骨格に沿ったメラノソームの移動速度として計測される事が一般的です。例えば文献[Wu et al. J. Cell Biol (1998) 143:1899-1918]ではメラノサイトの細胞内に存在する一部のメラノソームを追跡しその動きをトレースするとともに、移動速度を測定しています。メラノソームの輸送障害はヒトやマウスの色素異常を引き起こす事が知られており、病態発症の理解という観点からも(正常細胞と病態細胞における)メラノソーム輸送動態の解析は当該研究分野における重要な研究課題です。
- 正常なメラノサイトにおけるメラノソーム輸送:
AVI動画, BMP画像 - Griscelli症候群メラノサイトにおけるメラノソーム輸送:
AVI動画, BMP画像 - Data使用にあたって
- 参考文献
- Kuroda, T. S., Ariga, H. and Fukuda, M. (2003) The actin-binding domain of Slac2-a/melanophilin is required for melanosome distribution in melanocytes, Mol. Cell. Biol. 23, 5245-5255.
- Kuroda, T. S. and Fukuda, M. (2004) Rab27A-binding protein Slp2-a is required for peripheral melanosome distribution and elongated cell shape in melanocytes, Nature Cell Biol. 6, 1195-1203.
緑色蛍光ラテックスビーズの結合・取り込み
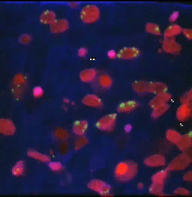
共焦点レーザー顕微鏡3次元観察画像例
緑色蛍光ラテックスビーズの結合・取り込み
(理化学研究所 大野博司 先生提供)
以下のデータは理化学研究所 大野博司 先生提供の細胞内外に結合・取り込まれた緑色蛍光ラテックスビーズの共焦点レーザー顕微鏡3次元観察画像です。そのビーズ数の自動認識や分布パターンの解析が求められています。大野先生には定量解析の学術意義として下記説明文を頂きました。
緑色蛍光ラテックスビーズが、赤く染色された細胞の表面に結合し、あるいは 一部細胞内に取り込まれている画像で、共焦点レーザー顕微鏡で取り込んだ画像の3次元再構築像です。この画像の場合は、例えば赤い細胞の表面に付着しているビーズ、中に取り込まれたビーズ、赤い細胞以外(見えていませんが細胞はびっしりと存在しており、その中に赤い細胞が点在しています)のところに付着しているビーズの数を自動定量することが考えられます。
- 3次元観察画像の回転動画:
MOV動画, 元画像(leica SP2の.rawデータ, 3カラーチャンネル, LAS AF LiteやImageJ(Bio-formats importer)等でI/O可能) - Data使用にあたって
刺激に応じて発光する細胞

時系列蛍光観察画像例
刺激に応じて発光する細胞
(理化学研究所 大野博司 先生提供)
以下のデータは理化学研究所 大野博司 先生提供の刺激に応じて発光する蛍光色素で染色された時系列細胞観察画像です。その発光パターンの自動解析や細胞間における発光関係の解析が求められています。大野先生には定量解析の学術意義として下記説明文を頂きました。
細胞内(subcellular)レベルではないのですが、刺激に応じて発光する蛍光色素でラベルされた細胞(青〜緑色で見えている1つ1つ)が散在しており、目では見えませんが、それぞれの細胞は細い細胞膜のチューブで繋がれています。そこで、画面内のある一つの細胞に刺激を与えると、それに応じて細胞は 赤〜白色に光ります。上に述べたように細胞膜が物理的に結合しているため、刺激はチューブを伝わって次々と連結した細胞に伝わり、このムービーのように、細胞は順次光ります。これら2つのムービーの場合、光る細胞を自動で追従して、その細胞間距離、刺激の伝達速度、伝達方向などのパラメータを解析することにより、刺激がどの細胞からどの細胞へ伝達したか、つまり、どの細胞とどの細胞がどのように物理的に連結しているのかを自動で解析したいと考えています。
- 時系列蛍光観察動画1: MOV動画, 元画像(DeltaVisionの.dvデータ, ImageJ(deltavision opener)等でI/O可能)
- 時系列蛍光観察動画2: MOV動画, 元画像(DeltaVisionの.dvデータ, ImageJ(deltavision opener)等でI/O可能)
- Data使用にあたって
細胞質細胞核分裂の4次元観察
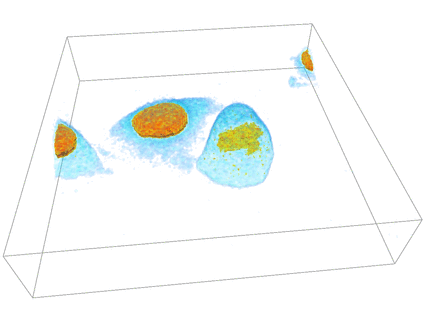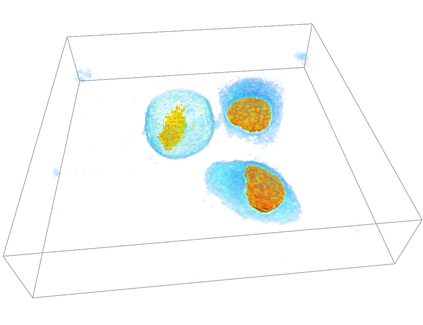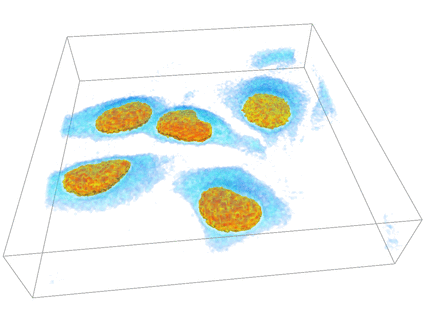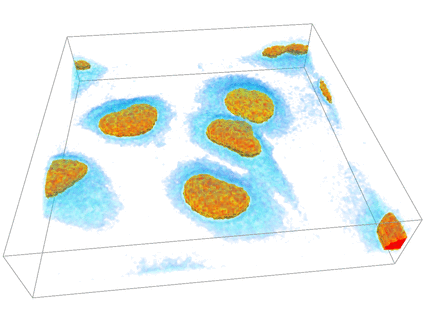
共焦点レーザー顕微鏡4次元察画像例
HeLa細胞の細胞質・細胞核分裂
(理化学研究所 生物基盤構築チーム 提供)
以下のデータは理化学研究所 生物基盤構築チーム 辻村さん観察のHeLa細胞の3次元時系列(4次元)観察画像です。個々の細胞・細胞核の自動認識・追跡や、その体積等の幾何統計量の定量解析法が求められています。
細胞内物流システムの観察画像ではありませんが、共焦点レーザー顕微鏡による典型的3次元時系列観察画像の例です。HeLa細胞にmCherry標識した核移行シグナル(mCherry-NLS)を用いて蛍光観察する事により細胞質部分と細胞核部分の輝度値の間に大きな差が現れて観察されます。この様に蛍光染色はある程度ターゲットの物質量に比例して輝度値が出る事が知られています。また、時間経過と共に、細胞分裂する細胞、観察領域内外を出入りする細胞が観察される事が通常なため、時系列データの定量解析には細胞/細胞核の個数・領域や時系列間の対応を堅固に計算する方法が必要な理由です。また、生きた細胞内の観察では、アグリゲーションと呼ばれる観察対象に意図しない蛍光タンパク質の塊が出来てしまう事があり、mCherryで細胞質を染めた場合に細胞質領域全体の認識・自動抽出を難しくします。
- 3次元時系列観察画像:
(複数のmulti-page tiff画像),
Size (350x350x43x17) voxel,
(x,y,z,time) pitch (0.286um,0.286um,0.5um,1 hour).
時刻01, 時刻02, 時刻03, 時刻04, 時刻05, 時刻06, 時刻07, 時刻08, 時刻09, 時刻10, 時刻11, 時刻12, 時刻13, 時刻14, 時刻15, 時刻16, 時刻17 - Data使用にあたって
- 参考文献
- X. Shu, N. C. Shaner, C. A. Tarbrough, R. Y. Tsien, and S. J. Remington, Novel Chromophores and Buried Charges Control Color in mFruits, Biochemistry, 2006, 45 (32), 9639-9647.
- R. D. Goldman and D. L. Spector, Live Cell Imaging: A Laboratory Manual, Cold Spring Harbor Laboratory Press, New York, 2005.
コレステロールプローブのエンドサイトーシス
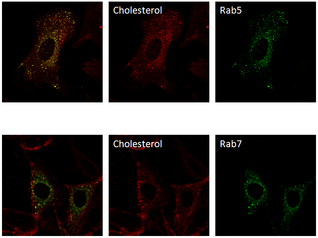
共焦点レーザー顕微鏡2次元観察画像例
コレステロールプローブ及びRab5、Rab7
(理化学研究所 生物基盤構築チーム 提供)
以下のデータは理化学研究所 生物基盤構築チーム 高橋さん観察の「CHO細胞における蛍光標識コレステロールプローブのエンドサイトーシスによる取り込み」を共焦点レーザー顕微鏡で観察した画像です。複数カラーチャンネルで別々の蛍光標識を観察し、その相関(左の画像)を、いままでにない新しい方法で自動解析する事が求められています。高橋さんには定量解析の学術意義として下記説明文を頂きました。下記高橋さんの論文では輝度値の相関係数を指標として用いています。さらに高度で細胞内観察画像に適した相関計算法の提案も期待されています。
コレステロールが細胞内でどのように輸送されるかを解析するために、コレステロールと似た挙動を示す蛍光標識コレステロールプローブを細胞に取り込ませて、共焦点レーザー顕微鏡で観察しました。また、蛍光標識コレステロール(赤)が細胞内のどのオルガネラに取り込まれるかを調べるために、初期エンドソームに局在するRab5(緑)、あるいは後期エンドソームに局在するRab7(緑)と、局在を比較しております。細胞内輸送の研究では、輸送される物質があるオルガネラから、別のオルガネラに移動したことを示すために、多色の蛍光で観察をして、色の重なりがどのように変化するかを解析する技術が多用されています(co-localizationの時間変化)。しかし、それらの解析の自動化は進んでいないため、多くの細胞を観察して解析することは困難です。そのため、自動解析する手法の開発が望まれています。
- コレステロールプローブのエンドサイトーシス観察画像:
(6枚のsingle page tiff画像),Size (512x512) pixel,(x,y) pitch (0.19um,0.19um).
元画像tiff6枚. - Data使用にあたって
- 参考文献
- M. Takahashi, M. Murate, M. Fukuda, S. B. Sato, A. Ohta, and T. Kobayashi, Cholesterol Controls Lipid Endocytosis through rab11, Molecular Biology of the Cell, Vol. 18, 2667-2677, 2007.
様々な条件下でのオートファゴソーム輝点
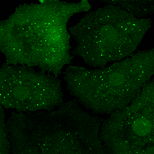
共焦点レーザー顕微鏡2次元観察画像例
様々な条件下でのオートファゴソーム輝点
(大阪大学 吉森保 先生提供)
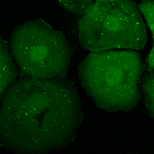
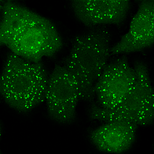
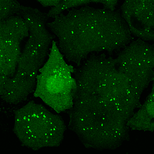
以下のデータは大阪大学 吉森保 先生提供の様々な条件下でのオートファゴソームマーカーのGFP-LC3を共焦点レーザー顕微鏡で観察した画像です。上の三つの画像は十分な栄養状態を観察したもので、下の三つの図は飢餓状態の細胞を観察したものです。また、左から右は異なる条件下で観察されています。オートファゴソームの輝点数を自動計算する事が求められています。吉森先生には定量解析の学術意義として下記説明文を頂きました。
オートファゴソームマーカーのLC3の間接蛍光抗体法やGFP-LC3イメージングで、オートファゴソーム数の定量を行っています。LC3は2つのフォームがあり、LC3-Iは細胞質に拡散しており、LC3-IIがオートファゴソーム膜に結合します。オートファゴソームはLC3の輝点(ドットないしリング)として確認されるので、オートファジーの亢進や抑制はLC3の輝点の数を数えることで定量されます。しかし、細胞質のLC3-Iの存在によりバックグラウンドが比較的高い、種々の理由でオートファゴソームではない小さな輝点や大きな輝点も現れる場合がある等の理由により、従来のソフトウェアでは自動検出が困難なので現在は目で見て数えています。自動的にオートファゴソームの輝点数を定量出来れば、データの客観性が増し大量のデータを迅速に数値化することが可能となります。
- 様々な条件下でのオートファゴソーム観察画像:
(6枚のsingle page tiff画像)
元画像tiff6枚. - Data使用にあたって
- 参考文献
- K. Matsunaga et al., Nature Cell Biol., inpress.
- Kabeya Y, Mizushima N, Ueno T, Yamamoto A, Kirisako T, Noda T, Kominami E, Ohsumi Y, Yoshimori T., LC3, a mammalian homologue of yeast Apg8p, is localized in autophagosome membranes after processing, MBO J. 2000 Nov 1;19(21):5720-8. Erratum in: EMBO J. 2003 Sep 1;22(17):4577.
- オートファゴソーム全般について
- Yoshimori T., Autophagy: Paying Charon's Toll, Cell 128: 833 - 6 (2007).
- Yoshimori T., Autophagy: a regulated bulk degradation process inside cells, Biochem Biophys Res Commun. 313: 453-8 (2004).
- 大阪大学 微生物研究所 吉森研究室のオートファジー解説.
オートファゴソーム形成因子
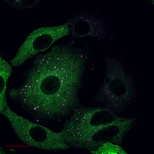
共焦点レーザー顕微鏡2次元観察画像例
オートファゴソーム形成因子
(大阪大学 吉森保 先生提供)
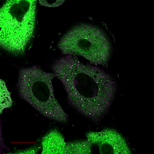
以下のデータは大阪大学 吉森保 先生提供のオートファゴソーム形成因子(LC3,オートファジー関連タンパク質その1,オートファジー関連タンパク質その2(Atg16L))を共焦点レーザー顕微鏡で観察した画像です。左の画像はLC3とオートファジー関連タンパク質その1の右の画像はオートファジー関連タンパク質その1とその2(Atg16L)を同時に観察したものです。オートファゴソームへ局在化する因子の相互依存関係を定量解析するために輝点の共局在率の自動計算法や新しい相関計算モデルが求められています。
- オートファゴソーム形成因子観察画像:
(2枚のsingle page (2 color channel) tiff画像)
元画像tiff2枚. - Data使用にあたって
- 参考文献
- K. Matsunaga et al., Nature Cell Biol., inpress.
- オートファゴソーム全般について
- Yoshimori T., Autophagy: Paying Charon's Toll, Cell 128: 833 - 6 (2007).
- Yoshimori T., Autophagy: a regulated bulk degradation process inside cells, Biochem Biophys Res Commun. 313: 453-8 (2004).
- 大阪大学 微生物研究所 吉森研究室のオートファジー解説.
(C) 2008~ Bio-research Infrastructure Construction Team, RIKEN, Japan. All rights reserved.